Consideriamo una reazione di dissociazione del sale in acqua:
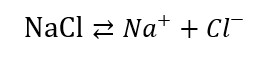
Facciamo finta che le moli all’inizio siano 3 mol di NaCl e all’equilibrio ce ne sono 2 moli di NaCl, avremmo che, in seguito alla dissociazione, ci sarà un numero di moli x di NaCl che non reagiscono e aumenteranno (sempre di un valore x) le moli degli ioni prodotti.
Possiamo scrivere il tutto in una tabella:
![]()

Dato che il numero di moli di NaCl sono 2 all’equilibrio ricaviamo il valore di x:
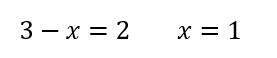
In questo modo abbiamo ricavato il numero di moli degli ioni:
![]()
Se si conosce il volume del contenitore si può calcolare anche la costante di equilibrio e il pH.
Se la reazione non fosse stata di dissociazione allora i reagenti sarebbero diminuiti di una quantità x e i prodotti sarebbero aumentati di una quantità x di moli.
