Dopo aver enunciato cos’è la chiralità possiamo parlare dell’isomeria: gli isomeri sono 2 molecole con gli stessi atomi ma differiscono per almeno un caratteristica ed in base a cosa differiscono sono classificati in modo diverso.
Gli isomeri più comuni sono gli isomeri costituzionali, cioè che differiscono solo per la posizione degli atomi. Esempi:
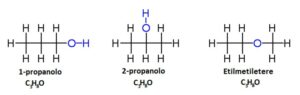
Gli isomeri sono detti conformazionali se possono diventare uguali facendo ruotare alcuni atomi di una delle molecole attorno a dei legami semplici, mentre se ciò non è possibile allora sono isomeri configurazionali. Se le due molecole sono immagini l’una l’immagine speculare non sovrapponibile dell’altra sono dette enantiomeri, altrimenti sono diastereomeri. L’ultimo tipo di isomeri sono gli isomeri atropoisomeri e vengono chiamati così se le due molecole possono diventare uguali velocemente a temperatura ambiente
